
今天借此机会,结合文献详细谈谈Li半电池扣电的弊端以及改善方法。顾名思义,Li半电池扣电,就是使用锂金属作为对电极(CE)和参比电极(RE),电极材料为工作电极(WE)的扣式电池体系,电流电压线接法如下所示,红的电流电压接在所谓的正极(电极材料,WE),蓝的电流电压接在锂金属负极(CE)上,此后进行充放电操作,一般情况下,我们默认得到的信息都是正极引起的,但是这种认识存在很大的问题,真实的情况锂金属对电极体系却存在二大缺陷,严重影响我们的判断。
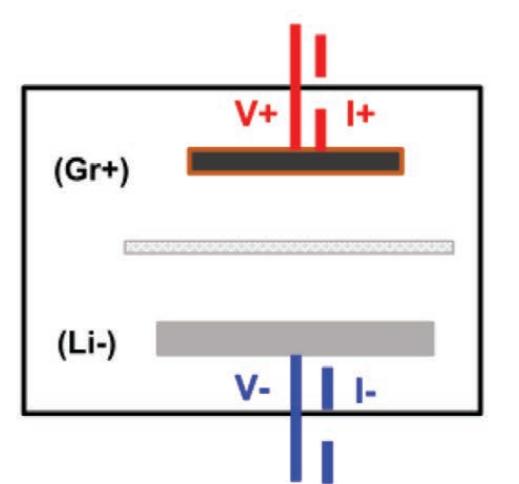
第一大缺陷:不稳定不均匀的SEI模导致锂枝晶和活性锂损失
众所周知,金属锂作为电位最低的材料,具有非常高的反应活性,几乎与所有的电解液成分发生反应,生成极为复杂的SEI膜。在半电池首次充电过程中,正极侧过来的锂离子在金属锂和电解液的界面上形成SEI膜,SEI具有实现扩散锂离子阻碍电子的功能,且不同位置上的SEI膜成分和形貌不尽相同。
在锂金属作为对电极的体系中,SEI膜要经历三个阶段,如下图所示,第一个阶段:正极侧过来的锂与电解液在锂金属表面在极快的时间内发生电化学反应,形成纳米级别的可保护锂金属对电极的有机无机电解质膜;第二阶段:锂沉积和脱出往返运动破坏SEI膜的结构,锂沉积时,沉积在锂金属表面的锂撑起SEI,在电流密度较大情况下,撑破SEI膜,导致漏出新鲜的电极与电极液再度形成SEI膜,锂脱出时导致锂金属表面与SEI之间形成孔隙,SEI发生坍塌;第三阶段:上一阶段的持续发生导致活性锂和电解液的消耗,导致库伦效率的降低,直至电池的完全失效。
 下图是锂金属和石墨为对电极的扣电测试结果,同样的正极材料NCM622,使用金属锂为对电极的数据极其差劲,在C1循环约50Cycle时候,容量只剩下33%,而使用石墨做对电极的情况下,无论是大倍率C1还是小倍率C10,容量保持率都是非常高且稳定的。拆开后的锂金属电极前后对比照片(b,c)上发现存在严重的锂枝晶,在隔膜上(d,e)的照片也验证了锂枝晶的存在污染了隔膜。
下图是锂金属和石墨为对电极的扣电测试结果,同样的正极材料NCM622,使用金属锂为对电极的数据极其差劲,在C1循环约50Cycle时候,容量只剩下33%,而使用石墨做对电极的情况下,无论是大倍率C1还是小倍率C10,容量保持率都是非常高且稳定的。拆开后的锂金属电极前后对比照片(b,c)上发现存在严重的锂枝晶,在隔膜上(d,e)的照片也验证了锂枝晶的存在污染了隔膜。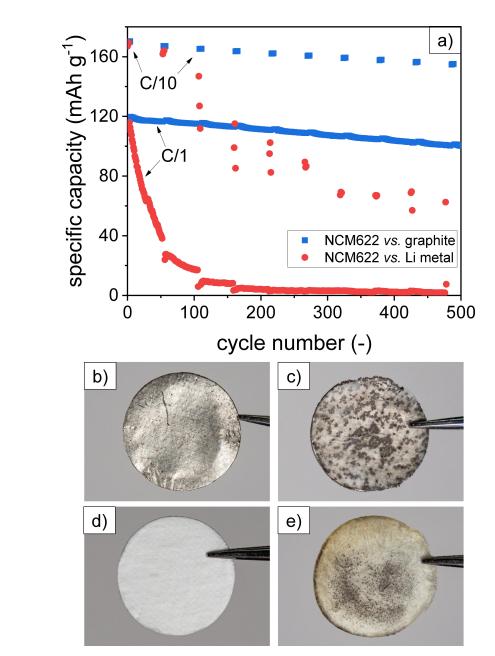 第二大缺陷:锂对电极贡献的极化占比高,影响工作电极的电化学特性半电池中锂金属对于全电池的阻抗影响非常大,下图是选择不同SOC下的EIS测试数据,从图中可以看出,不同锂金属的Rct阻抗值都会比工作电极的石墨大,正是由于这种原因,所以在测试时候,我们得到的数据很难认为都是工作电极引起的,甚至有些时候不同的工作电极的性能发生了改变,但是从总的测试数据得不到反馈的相应信号,这都是由锂对电极引起的。
第二大缺陷:锂对电极贡献的极化占比高,影响工作电极的电化学特性半电池中锂金属对于全电池的阻抗影响非常大,下图是选择不同SOC下的EIS测试数据,从图中可以看出,不同锂金属的Rct阻抗值都会比工作电极的石墨大,正是由于这种原因,所以在测试时候,我们得到的数据很难认为都是工作电极引起的,甚至有些时候不同的工作电极的性能发生了改变,但是从总的测试数据得不到反馈的相应信号,这都是由锂对电极引起的。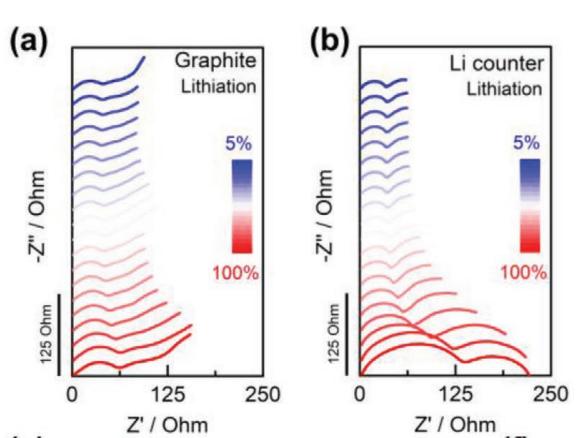
由于锂对电极极化的影响,在充放电过程中测量出来的Ecell明显偏离正常的Ewe电位。
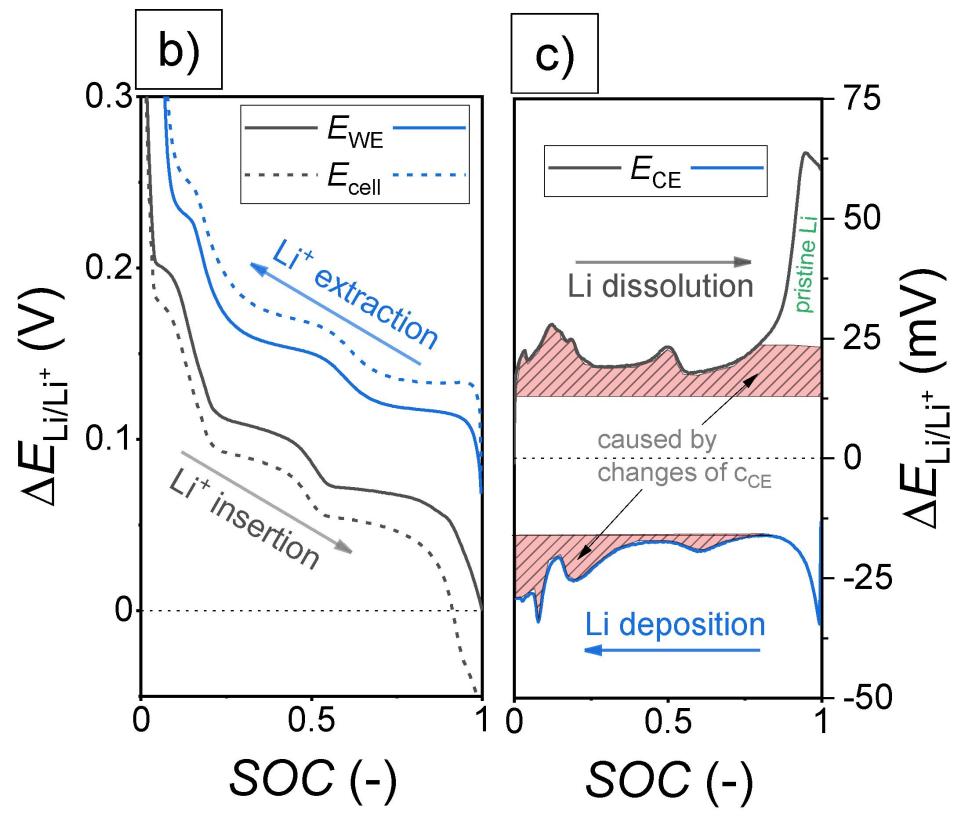
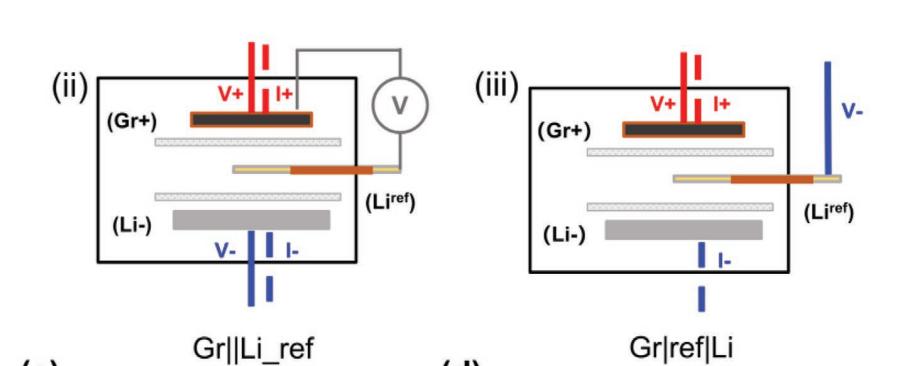
常见的方法有两种,一种是选择给锂半电池加参比电极,如下图所示,第一种可以用于监测实时状态下的工作电极电位,第二种就实现对工作电极测试的精准控制;另外一种是对于长期的测试,尽可能选择膨胀变化更小的石墨对电极,以减少对电极对工作电极的影响。
需要提醒的是锂半电池扣电并非一无是处,它仍然可适用于小电流密度或者短期的验证工作,只是对于高容量高倍率的验证工作有其他结构的扣电可以做的更好。
文献参考
[1]Adv. Energy Mater. 2023, 13, 2204077
[2]Electrochemical Characterization of Battery Materials in 2-Electrode Half-Cell Configuration: A Balancing Act Between Simplicity and Pitfalls
[3]Batteries & Supercaps 2021, 4, 1310–1322
