在电化学体系分析中,我们常常需要借助参比电极来分析工作电极的信息或者解耦正负极的电极状态,不过选择合适的参比电极对分析才具有稳定定量的价值。
从定义上来讲,参比电极(Reference Electrode,RE)是指一个电势已知、接近于理想非极化的电极。通过监测其他电极与参比电极之间的电压,来分析在不同条件下的电极电位,需要注意的是,工作电极上只有非常微弱的电流通过,相当于电压表的一端接在其上面,另一端接在了工作电极上。
关于理想非极化电极的内容介绍,可以参看这篇文章。
对于参比电极来说,通常需要有满足几个基本要求1、电极电位稳定电极电位在不同成分电解液,不同局部电场强度,不同温度等等环境下能够保持稳定的电位值,且电极电位不随时间的变化而变化。2、可逆性高,不易极化
参比电极在经历电流的冲击,仍然能够保持稳定的电极电位不变,不易发生极化现象,也就是说抗干扰能力强,举个例子,参比电极就像海上的灯塔坐标,无论从哪个方向来的台风吹到塔体,它仍然能够保持稳定的姿态和固定的位置,这也是它可以作为位置参考的核心要求。3、无污染无干扰
参比电极不能污染待测量的电化学体系,不能污染电解液,不会对工作电极或其他组成构成干扰,也可以说要求其具有一定程度的“惰性”。
在电化学体系中常用的参比电极有氢标电极,饱和甘汞电极,银氯化银电极,一般根据电解液PH选择不同的参比电极体系,如下图所示,要测量一个研究电极的电极电位,往往把研究电极与参比电极组成回路,采集电压就能计算出研究电极的电位值。

在电化学体系中,一般电极电位都是相对于氢标电极而言的,而在锂电池研究中,一般电极材料的电极电位都是相对于锂金属参比电极,为什么会选择锂作为锂电池的参比电极呢?
高容量电池在测试过程中本身就具有一定的风险性,那么放置在电池中间的参比电极必须保证不会导致电池的内部短路等异常。
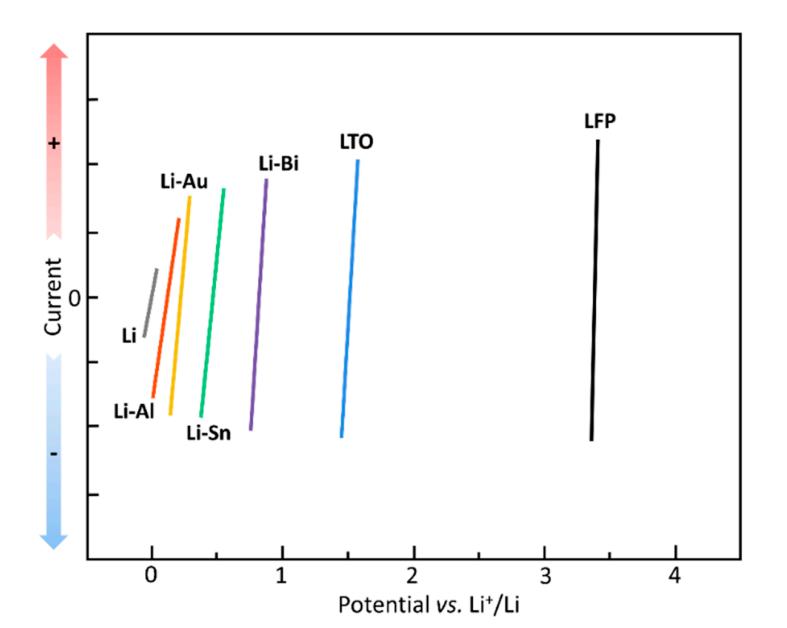
目前锂电池的参比电极一般集中在锂金属、锂合金和锂氧化物。锂金属电位在0V左右,由于操作简单和快速的动力学属性成为了首选材料,作为可以达到最高的锂含量的参比电极,锂金属也具有较长的使用寿命和准确性,但是在其表面形成的SEI膜会对测试造成一定程度上的影响;锂合金电位在0-1V之间,它作为参比电极时,相对于锂金属,高一点的电位能够缓解与电解液反应生成SEI的过程,但是具有多段电位和体积变化大的特征也限制了其在锂电池上的使用;锂氧化物电位在1-4V之间,高电位使其具有更广泛的适用性,同时该类参比电极的制作过程会相对复杂些。
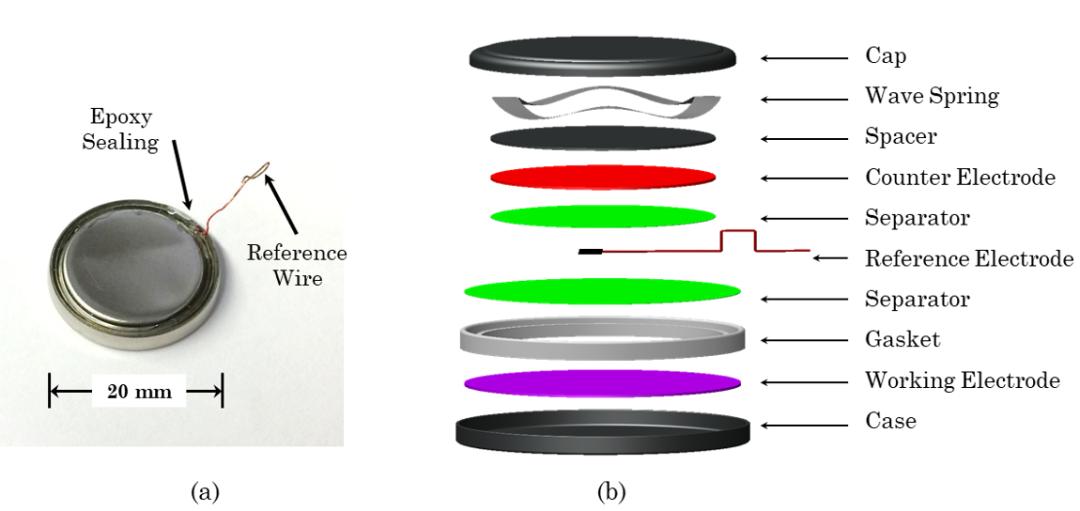
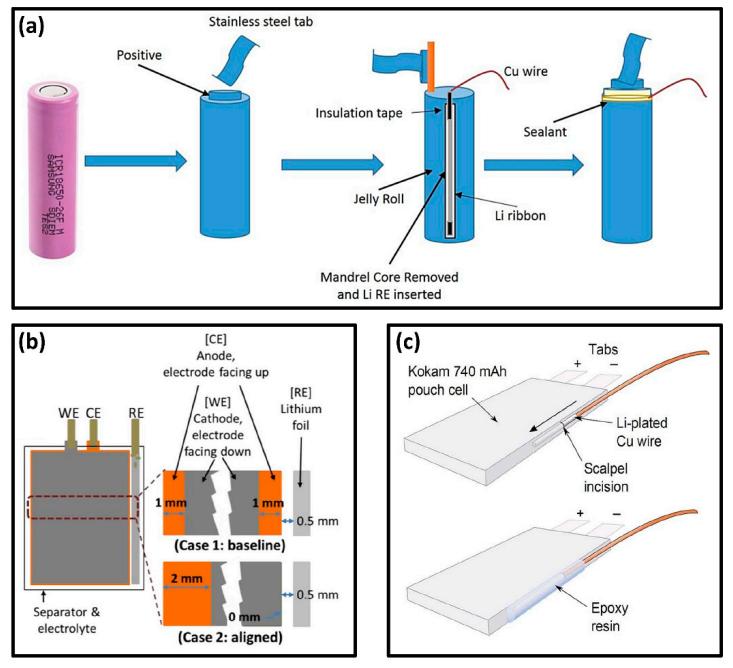
如下图所示,无论是在扣电,圆柱,软包和铝壳电池,都能够成功顺利地制作成三电极的电池,在这当中,需要确定好合适的参比电极尺寸和位置,以减少对电池的影响。
作为在电化学领域中重要的分析工具,参比电极能够让我们更清晰地认识电池,加深对电池机理的理解,但是真正意义上做出一类长寿命高稳定的参比电极仍然是一道难题,希望借助设备和工艺的发展,参比电极能够更好地发挥作用,助力做出更安全更长寿命的电池。
参考文献
Batteries 2019, 5, 12; doi:10.3390/batteries5010012
